بیماریها و راه درمان, پیشگیری بهتر از درمان, دارونامه , تغذیه سالم , فرناز اخباری
به گزارش سایت mayoclinic.org
سندرم کبدی ریوی یک بیماری غیرشایع است که ریههای افراد مبتلا به بیماری کبدی پیشرفته را تحت تأثیر قرار میدهد. این سندرم ناشی از بزرگ شدن (متسع شدن) رگهای خونی در ریهها و افزایش تعداد آنهاست که باعث می شود اکسیژن به درستی در گلبولهای قرمز خون جذب نشود. در نتیجه ریهها نمیتوانند مقدار کافی اکسیژن را به بدن برساند، که منجر به کاهش سطح اکسیژن (هیپوکسمی) میشود.
هنگامی که کبد به درستی کار نمیکند، ممکن است رگهای خونی در ریه ها متسع شوند. اگر شدید باشد، ریهها توانایی خود را در انتقال اکسیژن به بدن از دست میدهند. این سندرم، سندرم کبدی ریوی HPS نامیده میشود و تقریباً در ۵-۳۲ % از بیماران مبتلا به زخم کبد (سیروز) ایجاد میشود.
سندرم کبدی ریوی یک عارضه نادر ریوی در بیماری کبد است.
برجستهترین علامت HPS معمولاً تنگینفس شدید و سطح پایین اکسیژن خون است. بیماران همچنین ممکن است متوجه شوند که نوک انگشتان آنها آبی میشود یا انگشتان آنها حالت چماقی به خود میگیرد. اکسیژن اضافی اغلب برای درمان علائم HPS مورد نیاز است، اما این ممکن است در موارد خفیفتر ضروری نباشد. در حال حاضر، تنها درمان شناخته شده برای HPS پیوند کبد است. پس از جایگزینی کبد در بیماران HPS، ریهها در عرض تقریباً یک سال به حالت عادی برمیگردند.

معرفی
اولین توصیف ثبت شده از سطح پایین اکسیژن در خون (هیپوکسمی) با اختلال عملکرد کبد توسط Flückiger در سال ۱۸۸۴ بود. تقریباً یک قرن بعد، در سال ۱۹۷۷، کندی و نادسون یک بیمار را با این یافتههای کلاسیک توصیف کردند و اصطلاح «سندرم کبدی ریوی» را به کار بردند.
امروزه HPS یک عارضه شناخته و نسبتاً شایع بیماری کبدی است که علل متفاوتی دارد (هر چند در کل بهعنوان یک بیماری نادر است، زیرا فقط بیماران مبتلا به بیماری کبدی میتوانند به آن مبتلا شوند).
HPS با سه ویژگی مشخص میشود:
(۱) بیماری کبد (اختلال عملکرد کبد یا فشارخون غیرطبیعی بالا در ورید بزرگ که خون را از روده به کبد و شاخههای آن میرساند (به نام فشارخون بالا).
(۲) افزایش خون عروقی که به ریهها وارد میشوند (اتساع عروقی داخل ریوی یا IPVDs است)
(۳) اکسیژنرسانی غیرطبیعی. اگرچه در مقالات گزارش شده تفاوتهایی وجود دارد و برخی در مورد آستانه اکسیژنرسانی صحیح برای شناسایی HPS مرتبط با بیماری بحث میکنند، یک گروه از محققان این بیماری را با گرادیان شریان آلوئولار بزرگتر مساوی ۱۵میلیمتر جیوه (و بیشتر از ۲۰ میلیمتر جیوه در بیماران بالای ۶۴ سال) تعریف کردند.
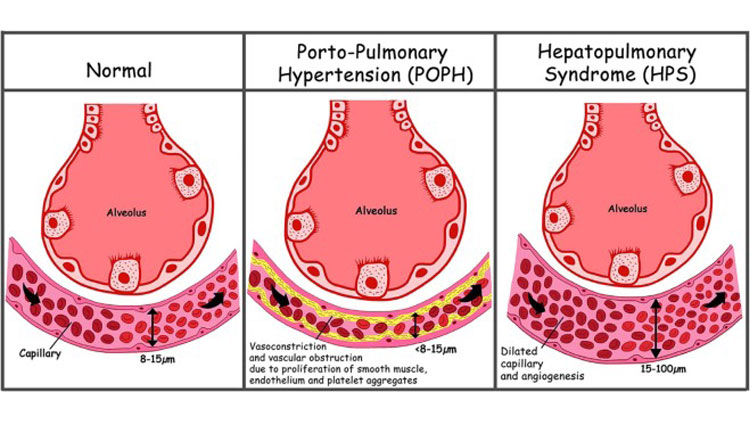
توجه به این نکته ضروری است که فشارخون بالای ریوی اغلب با سندرم کبدی ریوی اشتباه گرفته میشود، اما اینها بیماریهای کاملاً متفاوتی هستند.
علائم و نشانهها
اکثر بیماران (۸۲%) در ابتدا با ویژگیهای بیماری کبدی خود مواجه بودند، در حالی که تعداد کمتری از آنان (۱۸%) ابتدا با شکایتهای ریوی مراجعه کردند. به طور کلی، شایعترین شکایت تنگینفس پیشرونده در حالت استراحت یا هنگام تمرین است که در ۹۵٪ بیماران گزارش شده و معمولاً بعد از سالها بیماری کبدی ایجاد میشود. با اینحال، با توجه به شیوع زیاد و اغلب چند عاملی بودن تنگینفس در بیماران مبتلا به سیروز، این شکایت به راحتی نادیده گرفته میشود و طبق گزارشات، بیماران HPS علائم تنفسی را به مدت ۴٫۸ سال قبل از تشخیص داشتهاند. علاوهبر این، این کاهش پیشرونده اغلب علیرغم عملکرد پایدار کبد وجود دارد.
شکایت خاصتر پلاتی پنه است تنگینفس در حالت عمودی و نشسته که هنگام خوابیدن بهبود مییابد (وضعیت خوابیده به پشت). این امر به نوبه خود با یافته عینی ارتودوکسی ( کاهش ۴ میلیمتر جیوه در فشار اکسیژن یا در اشباع در هنگام تغیر پوزیشن از حالت خوابیده به حالت ایستاده ارتباط دارد ) که در ۸۸ درصد بیماران HPS رخ میدهد.
سایر تظاهرات بالینی HPS عبارتند از:
- آنژیومات عنکبوتی (عروق خونی کوچک و متسع که در نزدیکی سطح پوست قرار گرفتهاند. (احتمالHPS 21%)
- گرفتگی انگشتان دست یا پا (احتمال HPS 78%)
- سیانوز (تغییر رنگ مایل به آبی غیرطبیعی پوست یا مخاط به دلیل بافتهای نزدیک سطح پوست با اشباع اکسیژن کم) (احتمال HPS100%)
توجه به این نکته ضروری است که عکس و سیتی اسکن قفسه سینه اغلب در HPS مشکل خاصی ندارند. فقدان ناهنجاریهای رادیوگرافی شواهد کافی برای رد HPS نیست.

همچنین باید توجه داشت که HPS فقط در بیماران مبتلا به اختلال شدید عملکرد کبد نیست. در حقیقت، بسیاری از بیماران مبتلا به HPS متوسط تا شدید عملکرد کبدی را به خوبی حفظ کردهاند.
علل
علت HPS نامشخص است و علت ابتلای برخی از بیماران مبتلا به بیماری کبدی به IPVD مشخص نیست. هیپوکسمی در HPS در درجه اول به دلیل محدودیت در میزان اکسیژن از ریهها به جریان خون (محدودیت انتشار) و ناهماهنگی بین هوای در حال حرکت از طریق ریهها و خون در حال حرکت در ریهها ناشی از وجود IPVDs (عدم تطابق تهویه و پرفیوژن) است.
بر این اساس، جهت یافتن علت HPS، بر علل ایجاد IPVDهایی که زمینهساز هیپوکسمی HPS هستند متمرکز شدهاند. کالبد شکافی در بیماران HPS تایید کرده است که رگهای خونی کوچک (مویرگها) در ریهها به شدت بزرگ شدهاند (متسع شده). این اتساع ممکن است ناشی از افزایش تولید یا اختلال در ترشح کبد از مواد شیمیایی باشد که باعث اتساع عروق خونی میشود و یا به علت کاهش تولید یا عدم حساسیت به ماده شیمیایی که معمولاً از کبد سالم ناشی از انقباض عروق خونی ایجاد می شودباشد.

اگرچه ماهیت این «عامل کبدی» نامشخص است، اما واضح است که در سطح رگهای خونی ریوی، نیتریک اکسید به عنوان عامل مهم اتسع عروق خونی (متسع شدن عروق) میباشد. NO ممکن است از چندین مسیر منتشر شود، از جمله التهاب ناشی از باکتریها و مواد باکتریایی که در بیماران مبتلا به سیروز (انتقال باکتری از روده) از روده به گردش خون منتقل میشود، که باعث جذب سلولهایی به نام ماکروفاژها به رگهای خونی ریوی میشود که NO14 را تولید و آزاد میکنند. علاوه بر این، در موشهای صحرایی مبتلا به HPS تولید بیش از حد مواد شیمیایی به نام اندوتلین -۱ را در کبد یافت شدکه باعث تولید و انتشار NO در ریهها میشود.
همانطور که درک ما از علت HPS بیشتر شود، مشخص میشود که این تغییرات با واسطه NO در اندازه عروق خونی ریوی به احتمال زیاد منجر به تغییر مزمنتری در ساختار خود عروق خونی میشود که به آن بازسازی عروق میگویند. به نوبه خود، این حالت ممکن است ناشی از عدم تعادل عوامل آزاد شده از کبد باشد که باعث تحریک و جلوگیری از رشد سلولهای رگهای خونی ریوی (سلول اندوتلیال) میشود، که هنوز مشخص نشده است.
جمعیت آسیبدیده
در میان افراد مبتلا به سیروز که در انتظار پیوند کبد ارتوتوپیک هستند (جایگزینی کبد فرد دریافتکننده با کبد اهدا کننده)، تقریباً ۷۰٪ از تنگینفس شکایت دارند، ۳۴ تا ۴۷٪ دارای اتساع عروقی داخل ریوی (IPVD) و ۵-۳۲٪ دارای HPS هستند.

HPS در کودکان و بزرگسالان، در مردان و زنان و در افراد از هر قومیتی رخ میدهد. با این حال HPS در افراد مبتلا به هیپرتانسیون پورتال غیرسیروزی با عملکرد سنتزی طبیعی کبد گزارش شده است (به عنوان مثال: هیپرپلازی رژنراتیو ندولار)، شایعترین علت سیروز است، اگرچه ارتباطی بین علت یا شدت سیروز با میزان شیوع و شدت HPS دیده نشده است.
اختلالات مرتبط
فشارخون بالای ریوی یکی دیگر از عوارض عروقی بیماری کبد است که اغلب با HPS اشتباه گرفته میشود. با این حال، سندرم کبدی ریوی و فشارخون بالا یک بیماری مشابه نیستند. اگرچه هر دو ناهنجاری عروق ریوی ناشی از بیماری کبدی هستند، HPS با اتساع عروق و هیپوکسمی مشخص میشود در حالی که فشارخون بالا ریه با انسداد یا تنگ شدن عروق خونی و فشار خون شریانی ریوی مشخص می شود.
تشخیص
از آنجا که تنگینفس در بیماریهای کبدی شایع است، HPS اغلب دیر تشخیص داده میشود یا اصلا تشخیص داده نمیشود. در موقع عدم وجود علایم فوق، اگر میزان اشباع اکسیژن کمتر از۹۶ باشد نشاندهنده HPS است.

تشدید تنگینفس در حالت ایستاده با حالت خوابیده به پشت(پلاتی پنه) و ارتودوکسی (فشار اکسیژن بیش از ۵ % یا ۴ میلیمتر جیوه در حالت ایستاده کاهش مییابد) فقط در ۲۵ % ا ز بیماران رخ میدهد اما مختص HPS است (تصور میشود که ناشی از توزیع مجدد گرانشی جریان خون به قسمتهای بازال ریهها یعنی جایی که اتساع عروقی شدیدتر است میباشد)، مانند گرفتگی یا سیانوز (در هر بیمار مبتلا به بیماری کبد).
بر این اساس، پزشکان باید در مورد بیماران مبتلا به بیماریهای کبدی و اشباع اکسیژن بیعلت کمتر از ۹۶% هر یک از موارد زیر: پلاتی پنه، ارتودوکسی، تغیرات کلابینگ یا سیانوز، HPSرا مد نظر داشته باشند. پس از ارزیابی ریوی، هر بیمار با گرادیان اکسیژن PaO2 <80 میلیمتر جیوه یا شیب آلوئولار-شریانی ۱۵میلیمتر جیوه که تابحال تشخیص خاصی برایش داده نشده، باید برای انجام آزمایش تشخیصی برای HPS احتمالی ارجاع داده شود.
روش تشخیصی برای HPS شامل آزمایش برای هر یک از سه جزء تعریف شده آن است. در ابتدا، شواهد مربوط به بیماری کبدی از طریق تصویربرداری شکمی برای ناهنجاریهای کبدی از جمله سیروز، و همچنین علائم جانبی فشارخون بالا، مانند بزرگ شدن وریدها (واریس) و یا بزرگ شدن طحال (اسپلنومگالی) انجام میشود. علاوه بر این، آزمایشات خونی که شواهد بیوشیمیایی اختلال عملکرد مصنوعی کبد را نشان میدهد، از جمله آلبومین، بیلیروبین و INR، که شواهدی برای سیروز است انجام میشود.

در مرحله بعد، شواهد IPVDs از طریق اکوکاردیوگرافی کنتراست (یا آزمایش شنت آلبومین جمع آوری شده)، و وجود افزایش شیب اکسیژن آلوئولار-شریانی با تجزیه و تحلیل گازهای خون شریانیABG) ) تعیین میشود.
با توجه به تأثیر مهم ارتودوکسی، در موارد مشکوک به HPS، توصیه میشود تجزیه تحلیل گازهای خونی تنها پس از ۱۵ تا ۲۰ دقیقه در حالت استراحت در حالت ایستاده انجام شوند.
- پالس اکسی متری. در پالس اکسی متری، یک سنسور متصل به انگشت یا گوش شما از نور برای تعیین میزان اکسیژن در خون شما استفاده میکند.
- تصویربرداری از قفسه سینه. اشعه ایکس، سیتی اسکن یا تصویربرداری اکوکاردیوگرام میتواند در سایر بیماریهای قلب یا ریه کمک کنده باشد.
ارزیابی و آزمایش بالینی
تمام آزمایشاتی که برای ارزیابی HPS احتمالی استفاده میشوند غیرتهاجمی هستند.
ارزیابی اولیه باید شامل برخی یا همه آزمونهای زیر باشد:
آزمایشات عملکرد ریوی
آزمایشات عملکرد ریوی در بیماران HPS معمولاً جریان طبیعی و حجم ریهها را نشان میدهد، اگرچه حجم ریه بیماران ممکن است با تجمع مایع در شکم (آسیت شدید) یا مایع اضافی در اطراف ریهها (پلورال افیوژن) کاهش یابد.

کاهش حرکت اکسیژن از ریهها به جریان خون (اختلال انتشار) یک یافته مکرر در HPS است که در ۸۳٪ از بیماران در یک مطالعه کیس سری وجود داشت، اما این یافته در افراد مبتلا به سیروز کبدی که HPS ندارند نیز مکرر است. در ۵۰-۷۰ درصد از بیماران مبتلا به سیروز رخ میدهد. با این حال، افراد HPS کاهش شدیدتری در ظرفیت انتشار دارند، که با میانگین پیشبینی شده DCLO ۵۵ درصد در مقابل ۷۲٪ در افراد مبتلا به سیروز کبدی که HPS ندارندمی باشد.
آزمایش پیادهروی شش دقیقهای و در صورت نیاز، تیتراسیون اکسیژن
یک آزمایش پیادهروی شش دقیقهای امکان ارزیابی عینی ظرفیت ورزش و هرگونه سطح پایین اشباع اکسیژن خون با ورزش را دارد. اگر اشباع فشار اکسیژن بیماران کمتر از ۸۸ شود، باید یک مطالعه تیتراسیون اکسیژن برای شناسایی و مطابقت با نیازهای اکسیژن انجام شود.
آزمایش عملکرد کبد
شامل تصویربرداری با سونوگرافی شکم و یا سیتی اسکن و برخی آزمایشات خون برای تعیین شدت بیماری کبدی بیمار است.

گازهای خون شریانی
برای این آزمایش، مقدار کمی خون از شریان مچ دست گرفته میشود. سپس سطح اکسیژن و دی اکسید کربن در خون تجزیه و تحلیل میشود تا مشخص شود که آیا ریههای بیمار به درستی عمل میکند یا خیر.
اکوکاردیوگرام
اکوکاردیوگرام که به سونوگرافی قلب نیز معروف است، تکنیکی است که از امواج صوتی برای گرفتن تصاویر از قلب استفاده میکند. در بیماران HPS، مقدار کمی آب نمک (محلول سالین) در حین اکوکاردیوگرام به ورید بازو تزریق میشود. این آزمایش کمک میکند تا مشخص شود که آیا رگهای خونی در ریهها متسع شدهاند؟ همانطور که میدانید این یکی از علائم بارز HPS است.
۲- اکوکاردیوگرافی دی ترانس توراسیک کنتراست سالین برای انتخاب IPVDها به یک تست انتخابی تبدیل شده است. میکرو حبابهای سالین با اندازه ۱۵-۱۸۰ um با مخلوط کردن ۱۰ میلیلیتر نرمال سالین با ۱۰ میلیلیتر هوا ایجاد میشوند و در طی اکوکاردیوگرافی معمولی ترانس توراسیک به صورت داخل وریدی تزریق میشوند. در عرض چند ثانیه، این حبابها در حفرههای قلب سمت راست ظاهر میشوند و در صورت عدم وجود IPVD ، در بستر مویرگی ریوی به دام میافتند و در نهایت جذب میشوند.
با اینحال، در HPS ، IPVD اجازه میدهد تا حبابها از بستر عروق ریوی عبور کنند و در نتیجه حبابهای قابل تشخیص در حفرههای قلب سمت چپ ایجاد میشود. از آنجایی که شانت داخل قلبی میتواند همان تأثیر را داشته باشد، زمان ظهور حباب سمت چپ به دقت کنترل میشود و اگر حبابها در عرض ۱ تا ۳ ضربان قلب ایجاد شوند، احتمالاً شانت داخل قلب است و اگر بعد از ۳ ضربان قلبی (معمولاً در داخل) ظاهر شود، داخل ریوی خواهد بود.

اسکن پرفیوژن ریه آلبومین تراکم بالا
گاهی اوقات یک اسکن کلی بدن آلبومین با برچسب تکنتیوم -۹۹ (اسکن MAA ) برای تعیین میزان ناهنجاریهای اکسیژناسیون بیمار تجویز میشود. برای این آزمایش، مقدار کمی ذرات ایمن و رادیواکتیو به نام Tc99m-MAA به بازوی بیمار تزریق میشود و سپس از یک دوربین تخصصی برای تشخیص این که این ذرات در کجای بدن میرسند، استفاده میشود. این یک روش اختصاصیتر برای آزمایش تشخیص وجود اتساع و شدت عروق خونی متسع در ریهها است.
به ویژه در بیمارانی که شواهدی از بیماری قلبی تنفسی همزمان وجود دارد، ممکن است از اسکن MAA برای تعیین میزان وجود HPS در ناهنجاریهای تبادل گاز استفاده شود.
در این روش، مجموعه ای از لیبلهای رادیوایزوتوپ آلبومین با دیامتر بین ۲۰ تا ۶۰ میلیمتر در ورید تزریق میشود. در افراد سالم، این ترکیبات آلبومین در رگهای خونی ریوی به دام میافتد و سینتی گرافی هستهای نشان اکثریت میزان جذب رادیوایزوتوپ ریوی را نشان میدهد.
با این حال، در صورت وجود IPVD یا شانت داخل قلبی، این سنگدانهها از مویرگهای ریوی فیلتر کننده رد شده و وارد گردش خون (سیستمیک) بدن میشوند و عمدتا در بسترهای مویرگی مغز، کلیه و کبد به دام میافتند. مقدار رادیوایزوتوپ شانت شده را میتوان اندازهگیری کرد و امکان محاسبه فراکشن شانت شده کل جریان خون ریوی خون میباشد.

سیتی اسکن قفسه سینه
این آزمایش برای ارزیابی سایر ناهنجاری هایی که ممکن است در اکسیژنرسانی غیرطبیعی نقش داشته باشند، انجام میشود. اگرچه رگهای خونی ریوی بهطور کلی متسع شدهاند، اما سیتی اسکن HPS را از بیماری کبدی بدون HPS متمایز نمیکند.
ویزیتهای بعدی اغلب شامل آزمایشهای عملکرد ریوی، تست پیادهروی شش دقیقهای، مطالعه تیتراسیون اکسیژن و گازهای خونی شریانی برای بررسی پیشرفت بیماری است.
درمانهای استاندارد
درمان
اکسیژن درمانی درمان مکمل اصلی تنگینفس ناشی از سطح پایین اکسیژن در خون است. پیوند کبد تنها درمان سندرم کبدی است.
پیوند کبد تنها درمان موثر برای HPS است، بهبود قابل توجه اکسیژنرسانی در اکثر بیماران طی یک سال پس از پیوند مشاهده میشود. بیماران نیاز به ارزیابی دقیق و پیگیری توسط متخصصان ریه و کبد قبل و بعد از پیوند دارند. اکسیژندرمانی طولانی مدت پایه اصلی درمان حمایتی برای HPS است و همچنین ممکن است در توانبخشی ریوی قبل و بعد از عمل نقش داشته باشد.
در بیماران HPS با غلطت اکسیژن کمتر از ۶۰ میلیمتر جیوه، میزان بقای ۵ ساله با پیوند کبد در مقایسه با بیمارانی که درمان حمایتی داشتند، بهطور قابلتوجهی بهتر بود. در نتیجه، شبکه مشترک پیوند اعضای بدن، اختصاص امتیازهای اضافی در سیستم اولویتبندی تخصیص اندام در بیماریهای کبدی مرحله آخر(MELD)، برای افراد HPS با اکسیژن کمتر از۶۰ میلیمتر جیوه، با هدف پیوند ظرف ۳ ماه را توصیه میکند.

از آنجا که هیپوکسمی در HPS پیشرونده است و پیش آگهی قبل از عمل و نتایج جراحی با شدت هیپوکسمی ارتباط تنگاتنگی دارد، بیماران HPS باید در اسرع وقت برای عمل پیوند در نظر گرفته شوند. همچنین، قابلتوجه است که در دهه گذشته، علاقه و تخصص روزافزونی در زمینه پیوند کبد ایجاد شده است، به نظر میرسد که این روش تأثیر مشابهی بر پیوند کبد از فرد فوت شده با HPS دارد.
تعدادی از عوارض مهم در مورد پیوند کبد برای HPS وجود دارد. اولاً، گزارش های متعددی از هیپوکسمی شدید پس از پیوند گزارش شده است که نیاز به تهویه مکانیکی طولانی مدت و تکنیکهای نوآورانه برای مدیریت هیپوکسمی بوجود آمد. همچنین، تعدادی از مراکز، افزایش عفونتهای بعد از عمل و نشت صفرا از بین مجاری صفراوی (نشت مجاری صفراوی آناستوموتیک) را ذکر کردهاند که به نظر محققان به دلیل هیپوکسمی، تاخیر در ترمیم زخم نیز خواهند داشت.
همچنین، تعداد زیادی از مطالعات لخته خون اولیه بعد از عمل در ورید پرتال و لخته شدن درشریان کبدی گزارش کردهاند ، احتمالاً به علت تولید بیش از حد گلبولهای قرمز (پلیسیتمی)ناشی از هیپوکسمی مزمن است. علاوه بر این، گزارشهایی از عود مجدد HPS پس از پیوند در نتیجه اختلال در پیوند ناشی از التهاب کبد و آسیب ناشی از تجمع چربی در کبد (استئاتوهپاتیت غیرالکلی ) یا هپاتیت C مکرر وجود دارد.
همچنین، گزارشی از رفع هیپوکسمی پس از پیوند و به دنبال آن افزایش فشارخون ریوی پیش رونده گزارش شده است. در نهایت، گزارشهای متعدد نشان داده است که کاهش ظرفیت انتشار ریهها در بیماران HPS ( با وجود بهبود اکسیژنرسانی) پس از پیوند بهبود نمییابد.

درمانهای تحقیقی
با توجه به کمبود اهداکننده اعضا و مرگومیر بالا در پیوند کبد دربیماران HPS، بسیاری از درمانهای پزشکی برای HPS پیشنهاد شده است، اما متأسفانه هیچ کدام موثر نبودند. نتایج مطالعات کوچک کنترلنشده درباره عواملی مانند سوماتوستاتین، آمیلترین، ایندومتیسین، تعویض پلاسما و آسپرین منفی بوده است. در برخی از مطالعات، سیر پتانسیل خود رادر موثر بودن نشان داده است.
در مطالعه آزمایشی تصادفی کنترل شده نورفلوکساسین منفی بود، و گزارشهای قبلی از پنتوکسیفیلین نتایج متناقضی داشته است. محصولات بازدارنده نیتریک اکساید مانند نیتروال آ رژنین متیل استر یا متیلن بلو بازدارنده NO نتایج متناقضی داشته است و نمیتوان آن را به عنوان درمان طولانی مدت مدنظر داشت. روش TIPSS شامل قرار دادن استنت فلزی قابل گسترش با مقاومت کم باآنژیوگرافی بین ورید کبدی و قسمت داخل کبدی ورید پورتال است. این روش در کاهش موقت فشار پرتال در عوارض خطرناکی مانند خونریزی واریسی مفید است. استفاده از TIPSS قبلاً بهعنوان یک درمان احتمالی در HPS پیشنهاد شده بود، اما نتایج در مطالعات و گزارشات متفاوت بوده است.
منابع:
۱- mayoclinic.org
۲- rarediseases.org