بیماریها و راه درمان, پیشگیری بهتر از درمان
دیابت یا بیماری قند (یا Diabetes Mellitus), یک اختلال سوخت و سازی (متابولیک) در بدن است. در این بیماری توانایی تولید هورمون انسولین در بدن از بین میرود یا بدن در برابر انسولین مقاوم شده و بنابراین انسولین تولیدی نمیتواند عملکرد طبیعی خود را انجام دهد. نقش اصلی انسولین پایین آوردن قند خون توسط سازوکارهای مختلف است. دیابت دو نوع اصلی دارد. در دیابت نوع یک، تخریب سلولهای بتا در پانکراس منجر به نقص تولید انسولین میشود و در نوع دو، مقاومت پیش رونده بدن به انسولین وجود دارد که در نهایت ممکن است به تخریب سلولهای بتای پانکراس و نقص کامل تولید انسولین منجر شود. در دیابت نوع دو مشخص است که عوامل ژنتیکی، چاقی و کمتحرکی نقش مهمی در ابتلای فرد دارند.
در دیابت، سرعت و توانایی بدن در استفاده و سوخت و ساز کامل گلوکز کاهش مییابد از اینرو میزان قند خون افزایش یافته که بهآن هایپرگلیسمی میگویند. وقتی این افزایش قند در دراز مدت در بدن وجود داشته باشد، سبب تخریب رگهای بسیار ریز در بدن میشود که میتواند اعضای مختلف بدن همچون کلیه، چشم و اعصاب را درگیر کند. همچنین دیابت با افزایش ریسک بیماریهای قلبی عروقی ارتباط مستقیمی دارد؛ لذا غربالگری و تشخیص زودرس این بیماری در افراد با ریسک بالا میتواند در پیشگیری از این عوارض مؤثر باشد. تشخیص و همچنین غربالگری دیابت با انجام آزمایش قند خون میسر است.
با انواع دیابت آشنا شوید:
دیابت دو نوع اصلی دارد که احتمالا در مورد نوع یک و دو بودن این بیماری چیزهایی شنیدهاید. در دیابت نوع یک تخریب سلولهای بتا در پانکراس منجر به نقص تولید انسولین میشود و در نوع دو مقاوت پیشرونده بدن به انسولین وجود دارد که در نهایت ممکن است به تخریب سلولهای بتای پانکراس و نقص کامل تولید انسولین منجر شود. در دیابت نوع دو عوامل ژنتیکی، چاقی و کمتحرکی نقش مهمی در ابتلای فرد دارند.
پایش قندخون
پایش قند خون به دو روش انجام میگیرد.
پایش قند خون توسط خود بیمار که به ان خود پایشی میگویند.
پایش قند خون توسط پزشک
در خود پایشی، قند خون توسط خود بیمار و با استفاده از یکی از انواع دستگاههای خانگی اندازهگیری قند خون انجام میگیرد در این روش گلوکز پلاسما اندازهگیری میشود و نمایانگر میزان کنترل قند خون در کوتاه مدت است. ارزیابی کنترل دراز مدت قند خون توسط پزشک انجام میگردد که از طریق درخواست آزمایش هموگلوبین A1C صورت میگیرد و نمایانگر میزان کنترل قند خون در دو تا سه ماه اخیر است. باید توجه داشت که این دو روش مکمل یکدیگرند و هیچیک جای دیگری را نمیگیرد. پزشک در نهایت با مرور اندازهگیریهای مکرر قند خون توسط بیمار و پاسخ آزمایشگاهی هموگلوبین A1C در خصوص نحوه ادامه درمان و مدیریت دیابت تصمیم میگیرد.
خود پایشی قند خون
یکی از وظایف بسیار مهم بیمار در کنترل بیماری دیابت، کنترل قند خون توسط خود بیمار با استفاده از دستگاه سنجش قند خون است. این روش به افراد دیابتی خصوصاً بیمارانی که انسولین تزریق میکنند یا بیمارانی که قند خون کنترل شدهای ندارند، کمک میکند که نظارت دقیقتری بر وضعیت خویش اعمال کنند و مسئولیت بیشتری برای اداره امور خود بر عهده گیرند. کنترل قند خون، مزایای فراوانی دارد. برای مثال کنترل قند خون قبل و ۲ ساعت بعد از صرف غذا به بیمار کمک میکند تا میزان تأثیر مصرف غذا بر قند خون را دریابد، پی بردن به این مسئله، بیمار را در انتخاب وعده غذایی مناسب یاری میدهد. همچنین میتوان با کنترل منظم قند خون در زمان فعالیت یا در زمان بیماری، میزان انسولین دریافتی را تنظیم کرد و بالاخره اینکه کنترل منظم قند خون، حس اعتماد بهنفس را در بیمار افزایش میدهد که توانسته از خود بهخوبی مراقبت کند.
دستگاه سنجش قند خون
انواع متعددی از این دستگاهها در ایران وجود دارد. علاوه بر انواع خارجی، نوع داخلی ان نیز تولید شدهاست. این دستگاهها دارای دو بخش الکترونیکی و نوار اندازهگیری قند خون هستند. نوارها یک بار مصرف و تنها در دستگاه مورد نظر قابل استفاده است در صورت عدم تولید هر کدام از این بخشها توسط شرکت سازنده، دستگاهی که در اختیار بیمار است غیرقابل استفاده میشود؛ از طرف دیگر انواع تقلبی و تاریخ مصرف گذشته نوارهای دستگاه سنجش قند در بازار ایران موجود است لذا بهترین گزینه برای انتخاب نوع دستگاه، مراجعه به لیست دستگاههای سنجش قند خون مورد تأیید وزارت بهداشت است. وزارت بهداشت دستگاههای مجوزدار و مورد تأیید این وزارتخانه را به همراه نوع گواهیهای معتبر آنها اعلام مینماید. در هر صورت با توجه به تعداد زیاد پایشگرهای گلوکز در دسترس، حضور یک آموزش دهنده مجرب دیابت جهت کمک به بیمار برای انتخاب نوع پایشگر مناسب بیمار و یادگیری طرز صحیح استفاده از ان دستگاه، الزامی است.
دستهبندی و سببشناسی دیابت
بیماری دیابت انواع مختلفی دارد که معمولاً در هنگام تشخیص متمایز میشوند؛ بنابراین تعیین نوع دیابت وابسته به شرایطی است که بیماری خود را در هنگام نشان بروز میدهد. در خیلی از بیماران به راحتی در یکی از دستههای مشخص دیابت جای نمیگیرند، مثلاً فردی که دچار دیابت بارداری شده ممکن است بعد از پایان بارداری کماکان دچار دیابت باقی بماند و لذا نوع دیابتش به نوع ۲ تغییر داده شود؛ بنابراین برای پزشک و بیمار برچسب زدن نوع دیابت نسبت به درک علت و سبب این بیماری و درمان مؤثر آن اهمیت بسیار کمتری دارد. تقسیمبندی قدیم دیابت به دو نوع وابسته به انسولین و غیر وابسته به انسولین که توسط NDDG در ۱۹۷۹ معرفی شد و در دهههای ۸۰ و ۹۰ بهطور گسترده به کار رفت مشکلاتی در درمان به وجود آورده بود که در نتیجه منجر به ارائه تقسیمبندی جدید دیابت توسط انجمن دیابت آمریکا به انواع: دیابت نوع یک، نوع ۲، سایر انواع و دیابت حاملگی در ۱۹۹۷ شد. این تقسیمبندی با وجودی که هنوز مشکلاتی دارد ولی مورد استفاده است.
مقایسه دیابت نوع یک و دو
| مشخصات |
دیابت نوع ۱ |
دیابت نوع ۲ |
| بروز |
ناگهانی |
تدریجی |
| سن بروز |
بیشتر کودکان |
بیشتر بزرگسالان |
| وضع بدن |
لاغر یا طبیعی |
معمولاً چاق |
| کتواسیدوز دیابتی |
شایع |
نادر |
| اتوآنتیبادی |
معمولاً وجود دارد |
ندارد |
| انسولین درونساز |
کم یا هیچ |
طبیعی، کاهشیافته
یا افزایش یافته |
مطابقت ژنتیکی در
دوقلوهای تکتخمی |
۵۰٪ |
۹۰٪ |
| شیوع |
~۱۰٪ |
~۹۰٪ |
دیابت نوع یک (وابسته به انسولین)
دیابت ناشی از واکنش ایمنی، (Type 1A) یک اختلال ناهمگون ناشی از جهشهای (اتوزومال مغلوب و وابسته به ایکس مغلوب) شناخته شده و همچنین توارث چندژنی/کمژنی است. این نوع دربرگیرنده ۵–۱۰ درصد از انواع دیابت است، قبلاً واژه دیابت وابسته به انسولین یا دیابت نوجوانی برای این نوع رایج بود. در این نوع از دیابت تخریب سلولی سلولهای بتا در پانکراس اتفاق میافتد. علت اصلی از دست رفتن سلولهای β، تخریب سلولی ناشی از واکنش ایمنی سلولی است. در پی این تخریب مارکرهایی در خون رها میشوند که شامل آنتیبادی علیه انسولین، اتوآنتیبادیهای گاد (GAD۶۵)، اتوآنتیبادی تیروزینفسفاتاز IA-۲ و IA-۲β است. این مارکرها ممکن است در ۸۵–۹۰٪ از مبتلایان دیده شود. ارتباطی میان اچالایهای خاص و این نوع از دیابت هم مشاهده شدهاست. این نوع دیابت در افراد دارای HLA-DQA و DQB و همچنین افراد دارای ژن DRBبیشتر مشاهده میشود. شیوع این نوع از دیابت در افرادی که بیماریهای خودایمن همچون بیماری گریوز، تیروئیدیت هاشیموتو، و بیماری آدیسون دارند بیشتر است. در پی تخریب سلولهای بتا توسط لنفوسیتها ترشح انسولین کاهش مییابد تا جاییکه انسولین موجود نمیتواند قند خون را تنظیم کند. معمولاً بعد از از دست رفتن ۸۰ تا ۹۰ درصد از سلولهای بتا است که هایپرگلایسمی اتفاق میافتد و دیابت ممکن است تشخیص داده شود. در این مرحله است که بیمار نیازمند انسولین خارجی میشود تا از بروز کتوز جلوگیری شود و هایپرگلایسمی و همچنین متابولیسم چربی و پروتئین کنترل شود. در حال حاضر فاکتور اصلی ایجادکننده دیابت نوع یک واکنش خودایمنی شناخته شدهاست. شواهد قوی نیز وجود دارند که عفونت ویروسی سلولهای بتای پانکراس را به عنوان اتیولوژی این واکنش ایمنی مطرح کردهاست. به این ترتیب که ویروس باعث ایجاد آنتیبادیهایی علیه پروتئین ویروس میشود که شعلهورکننده یک واکنش خود ایمن علیه سلولهای بتای مشابه است. دیابت ناشی از ایمنی معمولاً در کودکی و نوجوانی اتفاق میافتد اما ممکن است در هر سنی مشاهده شود.
دیابت ایدیوپاتیک:در مواردی از دیابت نوع یک علت مشخصی برای بروز آن یافت نشده و در این گروه طبقهبندی میشوند. بعضی از این بیماران دچار کمبود انسولین دائمی و مستعد کتواسیدوز هستند ولی هیچ شواهدی از واکنشهای خودایمن در آنها مشاهده نمیشود. تعداد کمی از بیماران دیابت نوع یک ایدیوپاتیک هستند و این وضعیت شیوع بیشتر در نژاد آفریقایی و آسیایی دارد. این نوع بیشتر ارثی است و وابسته به اچالای نیست. نیاز به انسولین خارجی در این بیماران پایدار نیست و میتواند گذرا و راجعه باشد.
دیابت نوع دو (غیروابسته به انسولین)
در دیابت نوع دو که ۹۰–۹۵٪ از بیماران دیابتی را شامل میشود، بدن نسبت به عملکرد انسولین دچار مقاومت میشود. این بیماران حداقل در ابتدای بیماری نقص انسولین نسبی (و نه مطلق) دارند. به این معنی که بدن فرد مبتلا انسولین تولید میکند و حتی ممکن است غلظت انسولین در خون از مقدار معمول آن نیز بیشتر باشد اما گیرندههای یاختهای فرد نسبت به انسولین مقاوم شده و در حقیقت نمیگذارند انسولین وارد سلولها شده و اعمال طبیعی خود را انجام دهد. این بیماران برای زنده ماندن نیاز به درمان دائم با انسولین خارجی ندارند. علل متعددی برای این وضعیت وجود دارد، مکانیزمهای جزئی بروز این وضعیت شناخته نشدهاست ولی مشخص است که تخریب اتوایمیون نقشی در بروز این بیماری ندارد.
دیابت نوع دوم در افراد چاق بیشتر دیده میشود و چاقی خود درجاتی از مقاومت به انسولین ایجاد میکند. درصد شیوع این بیماری در زنان بیش از مردان است. در این نوع از دیابت کتواسیدوز به ندرت خودبهخود ایجاد میشود بلکه در پی یک استرس همچون بروز یک بیماری یا عفونت ایجاد میشود. این نوع از دیابت معمولاً سالها تشخیص داده نشده باقی میماند چرا که هایپرگلایسمی (افزایش قند خون) به تدریج ایجاد میشود و در اوایل در حدی نیست که علائم کلاسیک دیابت را نشان دهد. با این حال این بیماران در معرض عوارض ماکروسکولار و میکرووسکولار دیابت هستند. مقاومت به انسولین ممکن است با کاهش وزن و درمان دارویی کمتر شود ولی به ندرت به حد طبیعی بازمیگردد. با اینکه اخیراً افزایش شیوع این نوع در کودکان و نوجوانان و سنین پایین دیده شده ولی در بیشتر موارد ریسک بروز این نوع با افزایش سن، چاقی و نبود یا کمبود فعالیت بدنی بیشتر شده و بیشتر در زنان با سابقه قبلی دیابت بارداری و افراد دارای فشار خون بالا یا اختلال چربی خون دیده میشود. نوع دو زمینه ژنتیکی قویتری نسبت به نوع یک دارد، با این حال ژنتیک دیابت نوع دو پیچیدهاست و هنوز به خوبی تعریف نشدهاست.
دیابت بارداری
هر نوع افزایش گلوکز خون در طی بارداری که به حد بالا ۵–۱۰٪ جمعیت برسد دیابت بارداری خوانده میشود. مشخص شدهاست که بارداری خود میتواند یکی از عوامل ایجادکننده دیابت باشد. این اثر با افزایش مقاومت بدن به انسولین و افزایش انسولین برای جبران این مشکل ایجاد میشود. حاملگی میتواند حتی نواقص خفیف ترشح انسولین را آشکار کند، این منجر به ایجاد عدم تحمل به گلوکز و دیابت بارداری میشود. از طرفی بعضی از افراد که از قبل دچار اختلال خفیف قند خون هستند با آزمایشهای غربالگری در طی بارداری تحت این گروه طبقهبندی میشوند. دیابت بارداری ۳–۸٪ از بارداریها را درگیر میکند و همچنین یکی از عوامل خطر برای نتایج بد بارداری است. همچنین این وضعیت مستقلاً میتواند باعث ایجاد دیابت نوع ۲ شود. تحقیقات نشان دادهاند که ۵۰٪ از این زنان طی ۲۰–۳۰ سال بعد دچار دیابت خواهند شد. در سالهای اخیر افزایش میزان ابتلا به دیابت بارداری مشاهده شدهاست. فاکتورهای ایجادکننده متعددی برای این افزایش مطرح شدهاند. شامل شیوع بالای چاقی در جوانان، بهبود بقای کودکان مؤنثی که وزن تولدشان در دو انتهای طیف وزن طبیعی تولد است. در بزرگسالی این کودکان دچار اختلال در عملکرد انسولین یا توانایی ترشح انسولین هستند که میتواند آنها را مستعد ابتلا به دیابت بارداری کند. دیابت بارداری میتواند منجر به عوارض جدی و گسترده برای مادر و نوزاد شود. این عوارض را میتوان با تشخیص و درمان مناسب کاهش داد، زنان دارای ریسک بالای ابتلا با آزمون ۷۵ گرمی تحمل گلوکز(OGTT) در اولین ویزیت بعد از بارداری آزمایش میشوند و آزمایش مجددی نیز در ۲۴ تا ۲۸ هفتگی بارداری انجام میشود. درمان دیابت بارداری در ابتدا با رژیم غذایی و فعالیت بدنی است و در صورت عدم پاسخ برای کنترل قند از درمان با انسولین استفاده میشود. این زنان پس از اتمام بارداری هم بهطور منظم مورد آزمایش قرار میگیرند.
انواع دیگر دیابت
نواقص ژنتیکی سلولهای بتا
انواع تکژنی دیابت گروه ناهمگونی (هتروژن) از دیابتیها را تشکیل میدهند که توسط یک جهش ژنتیکی ایجاد میشوند و با اختلال ترشح انسولین مشخص میشوند. تخمین زده میشود که ۵٪ از تمام انواع دیابت ناشی از این جهشها است، با این حال تشخیص دقیق اهمیت زیادی در درمان، پروگنوز و ریسک در افراد خانواده دارد. شایعترین نوع معمولاً با بروز افزایش قند در سنین پایین (زیر ۲۵ سال) مشخص میشود که دیابت بارز شده در بلوغ جوانان (MODY) نامیده میشوند. توارث این نوع اتوزومال مغلوب است، اختلالات در شش محل ژنی تاکنون برای این بیماری شناخته شده که شایعترین آن (۵۰–۷۰٪ موارد) روی کروموزم ۱۲ در فاکتور رونویسی هپاتیک، معروف به جهش HNF-۱α است. شکل دوم مربوط به جهش ژن گلوکوکیناز روی کروموزوم ۷p است که منجر به تولید مولکول معیوب گلوکوکیناز که عامل تبدیل گلوکز به گلوگز-۶-فسفات و تحریک ترشح انسولین است میشود. به علت این جهش مقادیر بالاتری از گلوکز لازم است تا منجر به ترشح انسولین حد طبیعی شود. فرم نادرتر جهش در سایر فاکتورهای رونویسی ژنی است شامل HNF-۴α، HNF-۱β، IPF-۱ و NeuroD۱ است. آزمایشهای ژنتیکی برای این نوع معمولاً در مواردی که سن بروز دیابت پایین است و علایم غیرمعمول بسته به دیابت نوع یک و دو مشاهده میشود یا سابقه خانوادگی قوی از این نوع وجود دارد توصیه میشود.
جهشهای نقطهای روی دیانای میتوکندریها که بهطور انحصاری از مادر به ارث میرسد این اختلالNIDDM نامیده میشود و با بروز دیابت و ناشنوایی مرتبط است. شایعترین فرم جهش موقعیت ۳۲۴۳ در tRNA ژن لوسین است. ضایعه مشابهی در سندرم ملاس (MELAS) دیده میشود، با این حال دیابت بخشی از این سندرم نیست.
اختلالات ژنتیکی که منجر به ناتوانی تبدیل پروانسولین به انسولین میشوند هم در خانوادههای کمی مشاهده شدهاند. یک صفت به صورت اتوزومال غالب به ارث میرسد. اختلال قند به وجود آمده در این حالت خفیف است.
دیابت شیرین نوزادی گروه ناهمگون دیگری از دیابتیها را تشکیل میدهد که تا ۶ ماهگی بروز پیدا میکند و یکی از هر ۲۰۰هزار تولد زنده را درگیر میکند. این اختلال با جهشهای متعدد که فرایند ارگانوژنز پانکراس، ایجاد سلولهای بتا و ساخت انسولین را مختل میکنند ایجاد میشود. این نوزادان برای سن بارداری کوچک(SGA) هستند و چربی زیرپوستی تحلیل یافته دارند.
اختلال ژنتیکی عملکرد انسولین
اختلالات ژنتیکی عملکرد انسولین شامل موارد نامعمولی از دیابت هستند. اختلال متابولیک ناشی از این جهشها میتواند از هایپرانسولینوما و هایپرگلایسمی خفیف تا دیابت شدید را شامل شود. بعضی از افراد دچار این نواقص ممکن است آکانتوز نیگرنس داشته باشند. زنان ممکن است صفات بدنی مردانه را نشان دهند و تخمدانهای بزرگشده کیستی داشته باشند. در گذشته این سندرم یک نوع مقاومت به انسولین شمرده میشد. لپرچانیسم و رابسونمندلهال دو سندرم در کودکان هستند که جهشهایی در گیرندههای انسولین و در نتیجه مقاومت شدید به انسولین دارند.
بیماریهای پانکراس برونریز
دیابت یکی از عوارض دیررس پانکراتیت مزمن است. تفاوتی که در این نوع دیابت وجود دارد تخریب کل غدد درونریز پانکراس است و لذا ترشح گلوکاگون هم کاهش مییابد، در نتیجه در این بیماران دیابتی احتمال بروز هایپوگلایسمی (افت قند خون) در پی درمان بیشتر میشود. غیر از پانکراتیت دیابت میتواند عارضه هر نوع صدمه وارد شده به پانکراس شامل عفونتها، جراحی برداشتن پانکراس و سرطان پانکراس نیز باشد.
اختلالات غدد درونریز
چندین هورمون با عملکرد انسولین میتوانند مقابله کنند که ترشح بیش از حد هر یک از آنها میتواند منجر به دیابت شود. معمولاً این وضعیت در افرادی دیده میشود که از قبل به علت نواقص ترشح انسولین مستعد دیابت باشند. افزایش هورمون رشد و کورتیزول از اختلالات شایع هورمونی منجر به دیابت هستند که افزایش عوارض و مرگ و میر قلبیعروقی در این بیماریها را به دیابت ناشی این اختلالات هورمونی نسبت دادهاند. تخمین زده شده که در ۱۶–۵۶٪ از بیماران آگرومگالی دیابت وجود دارد و در کوشینگ شیوع دیابت به ۲۰–۵۰٪ میرسد.
دیابت در اثر داروها یا مواد شیمیایی
تخریب برگشتناپذیر سلولهای بتا در مواردی نادری در پی مصرف واکور (نوعی سم ضد موش) یا پنتامیدین وریدی ممکن است اتفاق بیفتد. برخی داروها هم میتوانند عملکرد انسولین را مختل کنند. به عنوان مثال نیکوتینیک اسید و گلوکوکورتیکوئیدها از این دسته هستند. بیمارانی که اینترفرون-آلفا میگیرند هم در مواردی دچار آنتیبادیهای ضد جزایر پانکراس یا نقص شدید انسولین شدهاند. برخی از داروهای پر کاربرد و نسبتاً بیخطر هم با افزایش ریسک بروز دیابت ارتباط دارند، شامل داروهای ضدفشار خون تیازیدی، استاتینها و بتابلاکرها. در مورد استاتینها مطالعات نشان میدهد که این افزایش ریسک بسیار اندک است و در حال حاضر این افزایش ریسک توجیهکننده قطع یا کاهش مصرف استاتینها نیست.
انواع نادر
عفونتها: برخی عفونتها همچون عفونتهای سرخک و سایتومگالوویروس مادرزادی و عفونت با کوکساکی ویروسهای سابتایپ ۳ و ۴.
انواع ناشی از ایمنی نادر: سندرم استیفمن، آنتیبادیهای ضد گیرنده انسولین
سایر سندرمهای ژنتیکی که با افزایش ریسک دیابت همراه هستند: سندرم داون، سندرم کلاینفلتر، سندرم ترنر، سندرم ولفرام، آتاکسی فردریک، بیماری هانتینگتون، سندرم لاورنس-مون-بیدل، دیستروفی میوتونیک، پورفیریا، سندرم پرادر ویلی
دستهبندیهای غیررسمی
آخرین تقسیمبندی رسمی دیابت توسط انجمن دیابت آمریکا در ۱۹۹۷ بود و با وجود مشکلاتی که دارد هنوز توسط مراجع اصلی، مورد تأکید و استفاده است با این وجود مدتهای مدیدی است که مشخص شده دیابت یک بیماری هتروژن است و شاید نیاز به تقسیمبندی جدیدی باشد. در ذیل به چند دستهبندی پیشنهادی اشاره میگردد:
دیابت نوع یک و نیم
دیابت خودایمن نهفته بزرگسالان (Latent Autoimmune Diabetes in Adults LADA) که ان را زیرگروهی از نوع یک میدانند که خصوصیاتی از دیابت نوع دو را هم دارد و از این رو که در بین دو نوع یک و دو قرار دارد انرا یک و نیم گفتهاند. اینان با سن کمتر از ۵۰، لاغرتر بوده، سابقه شخصی یا خانوادگی بیماریهای خودایمن داشته و با احتمال بالا در عرض ۵ سال پس از شروع بیماری، نیازمند انسولین خواهند گشت.
دیابت نوع ۳
شواهد اپیدمیولوژیکی و علمی نشانگر وجود ارتباط پاتوفیزیولوژی مشترک بین دیابت نوع ۲ (T2DM) و بیماری آلزایمر (AD) میباشد. تا آنجا که این فرضیه مطرح شدهاست که AD ممکن است “دیابت نوع ۳” باشد. دانشمندان در پی تحقیقات خود دریافتند که مقاومت به انسولین که شاه علامت مکانیزم دیابت است، در مغز هم رخ میدهد. این نکته از آنجا مهم است که بر خلاف اعضای وابسته به انسولین یعنی عضله، کبد و بافت چربی، مغز جزو ارگانهای غیر وابسته به انسولین است و جهت ورود گلوکز بدرون سلولهای عصبی نیازی به وجود انسولین نمیباشد و در ادامه متوجه شدند که این مقاومت با بروز بیماری الزایمر همراه است. مطالعه دیگری نشان داد که الزایمر میتواند بدون بالا رفتن قند خون (هیپرگلایسمی) در مغز بروز کند.
علاقمندی رو به رشدی در تشخیص نقش ژنهای انسولین و فاکتور رشد مشابه انسولین (IGF) و گیرندههای مرتبط با آن (T2DM) در بروز اختلالات شناختی، آلزایمر و ضایعات اسکلتی عصبی ناشی از آلزایمر و ضایعات Aβ در مغز وجود دارد. این ارتباط نشان میدهد که انسولین و مکانیسم سیگنالینگ انسولین برای بقای نورونها بسیار مهم هستند و مطالعات نشان داد که کاهش رشد مغز و افزایش فسفوریلاسیون tau در موشهای دارای نقص در گیرنده انسولین ۲ و گیرنده انسولین عصبی وجود دارد. از سوی دیگر، مطالعات مختلف نشان دادهاند که لیگاندهای قابل استخراج آمیلوئید بتا (ADDL) هم ممکن است مسئول بروز این پدیده باشد. ADDL الیگومرهایی مشابه در مورفولوژی و سایز به پریونهای مرتبط با بیماریهای نورودژنراتیو هستند. ADDLها ممکن است باعث کاهش سطح انسولین و مقاومت به انسولین در مغز بیماران آلزایمری شوند. نتیجهگیری میشود که اصطلاح “دیابت نوع ۳” دقیقاً نشان دهنده این واقعیت است که بیماری آلزایمر نوعی دیابت است که به صورت انتخابی مغز را درگیر میکند و دارای ویژگیهای مولکولی و بیوشیمیایی است که با دیابت نوع ۱ و نوع ۲ همپوشانی دارد.
دستهبندی پنج خوشهای جدید
در این تقسیمبندی دیابت به جای دو نوع یک و دو در تقسیمبندی انجمن دیابت آمریکا به پنج خوشه (Cluster) به عنوان زیرگروههای دیابت دستهبندی شدهاند. هدف این است که بتوان برای هر خوشه درمان مناسب را در زمان مناسب شروع کرد تا به نتایج بهتری نایل شویم. در ۲ مارس ۲۰۱۸ گروهی از پژوهشگران در سوئد و فنلاند اعلام کردند که بر اساس تصویر پیچیدهتری که آنها از دیابت کشف کردهاند، دورهٔ جدیدی در تجویز داروها برای دیابت آغاز شدهاست. این دانشمندان میگویند بیماری دیابت دارای پنج نوع مختلف است که درمان متناسب برای هر نوع میتواند جداگانه تهیه و تجویز شود. آنها میگویند این نتیجهگیری آیندهٔ مراقبت از دیابت را دگرگون خواهد کرد اما تغییرات در درمان سریعاً صورت نخواهد گرفت. این مطالعه توسط مرکز دیابت دانشگاه لوند در سوئد و مؤسسهٔ پزشکی مولکولی فنلاند بر روی ۱۴٫۷۵۵ بیمار همراه با بررسی دقیق خون آنها انجام شدهاست. نتایج منتشر شده در دیابت و اندوکرینولوژی لنست نشان میدهند که بیماران میتوانند به پنج گروه متمایز تقسیم شوند:
گروه اول: این گروه را دیابت خودایمنی شدید (severe autoimmune diabetes SAID) مینامند. اینان در سنین پایین مبتلا شده، شاخص توده بدنی انان(BMI) کم است، کمبود انسولین دارند و دارای اتو انتیبادیهای ضد گلوتامیک دکربوکسیلاز (glutamate decarboxylase autoantibodies GADA) که شاخصه نوع یک کلاسیک است، میباشند لذا به دیابت نوع یک شبیه است و با آنکه بدن بیمار خصوصیات یک بدن سالم را نشان میدهد، ولی به خاطر عارضهٔ بیماری ایمنی توانایی تولید انسولین را ندارد.
گروه دوم: این خوشه دیابت با کمبود شدید انسولین (severe insulin deficient diabetes SIDD) نام دارد. این بیماران به بیماران گروه اول بسیار شبیه هستند ولی با این تفاوت که شاخصه خودایمنی یعنی اتو انتیبادیهای ضد گلوتامیک دکربوکسیلاز (glutamate decarboxylase autoantibodies GADA) را در سرم خود ندارند؛ لذا آنان توانایی تولید انسولین را ندارد ولی این اختلال از نقص در سیستم ایمنی بدن آنها ناشی نمیشود.
گروه سوم: این خوشه دیابت با مقاومت انسولینی شدید (severe insulin resistant diabetes SIRD) نام گرفتهاست. بیمارانی که در این گروه قرار میگیرند بهطور کلی دچار عارضهٔ اضافهوزن هستند؛ و هرچند بدن این بیماران انسولین کافی تولید میکند، اما به دلیل مقاومت انسولینی شدید، بدن دیگر قادر به واکنشدهی به این هورمون نیست.
گروه چهارم: این خوشه دیابت خفیف مرتبط با چاقی (mild obesity related diabetes MOD) نام دارد که بیشتر در افرادی با اضافهوزن بالا مشاهده میشود، ولی این گروه، فاقد مقاومت واضحی نسبت به انسولین هستند و لذا از نظر متابولیک نسبت به بیماران گروه سوم به وضعیت معمولی نزدیکتر هستند.
گروه پنجم: دیابت خفیف مرتبط با سن (mild age related diabetes MARD) است؛ این خوشه معمولاً در افراد با سن بالا دیده میشود و جز سن بالا، مثل خوشه چهار، اختلال متابولیک واضحی ندارد و لذا علائم این گروه در مقایسه با بیماران سایر گروهها خفیفتر است.
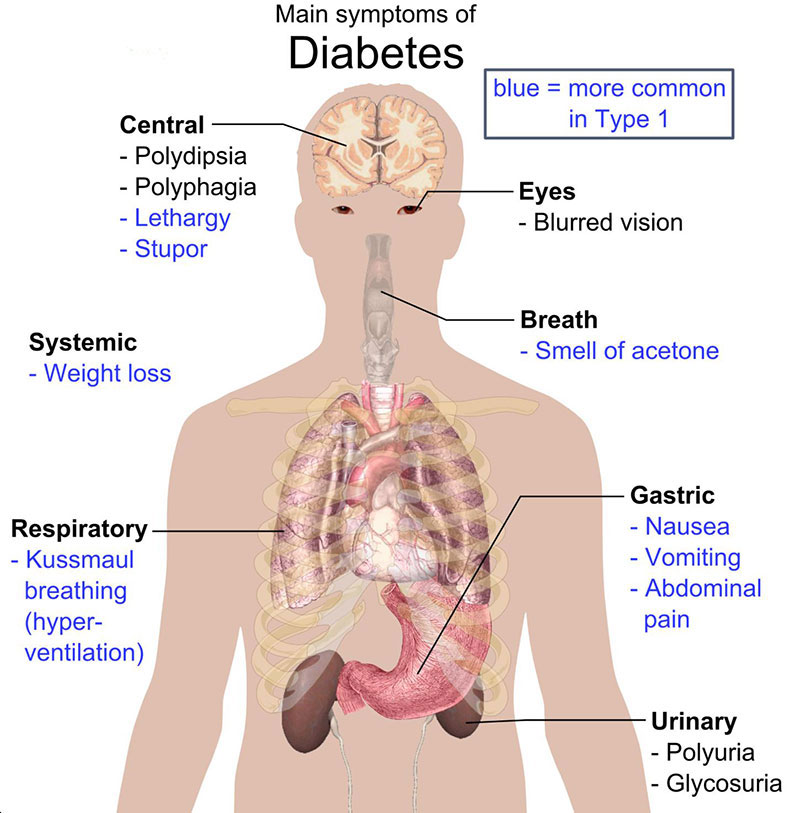
علائم و نشانهها
در مراحل ابتدایی ممکن است دیابت بدون علامت باشد. بسیاری از بیماران بهطور اتفاقی در یک آزمایش یا در حین غربالگری شناسایی میشوند. با بالاتر رفتن قند خون، علائم دیابت آشکارتر میشوند. پرادراری، پرنوشی، پرخوری، کاهش وزن با وجود اشتهای زیاد، خستگی و تاری دید از علایم اولیه شایع دیابت است. بسیاری از بیماران در هنگام تشخیص بیماری چندین سال دیابت داشتهاند و حتی دچار عوارض دیابت شدهاند. در کودکان دچار دیابت نوع یک علایم معمولاً ناگهانی بارز میشوند، این افراد معمولاً قبلاً سالم بوده و چاق نبودهاند. در بزرگسالان این علایم معمولاً تدریجیتر بارز میشوند. عارضه کتواسیدوز میتواند به عنوان علامت شروعکننده بیماری هم در دیابت نوع یک بارز شود. در دیابت نوع دو معمولاً فرد تا سالها بدون علامت است. علایم معمولاً خفیف هستند و بهطور تدریجی بدتر میشوند. در نهایت فرد دچار خستگی مفرط و تاری دید شده و ممکن است دچار دهیدراتاسیون شود. در این بیماران عارضه کتواسیدوز به علت تولید انسولین اندک کمتر دیده میشود. با این حال قند خون میتواند به مقادیر بسیار بالایی افزایش یابد و فرد دچار عارضه شوک هایپراوسمولار شود.
نتیجه یک مطالعه نشان میدهد که استرس و افسردگی، احتمال سکته مغزی و مرگ ناشی از بیماریهای قلبی عروقی را در بیماران مبتلا به دیابت بیش از دو برابر افزایش میدهد.
عوارض
حاد
کتواسیدوز دیابتی: این عارضه با سه مشخصه بیوشیمیایی کتوز، اسیدوز و هایپرگلیسمی متمایز میشود. کتواسیدوز دیابتی میتواند به عنوان علامت اولیه در دیابت نوع یک بارز شود ولی معمولاً در بیماران تشخیص داده شده دیابت در موقعیتهایی که میزان انسولین خون کمتر از نیاز بدن است ایجاد میشود، همچون فراموش کردن دوز انسولین یا افزایش ناکافی دوز انسولین در وضعیتهای استرس همچون بیماری و جراحی. کتواسیدوز دیابتی با علایم تنفس کاسمال، نفس با بوی کتون، تهوع و استفراغ، دهیدراتاسیون و درد شکم یا کاهش سطح هوشیاری خود را نشان میدهد. درمان این وضعیت درمانی تخصصی است که معمولاً نیاز به بستری اورژانس در بخش مراقبتهای ویژه دارد. رکن اصلی درمان هیدراتاسیون و کنترل قند و اسیدوز است.
سندرم هایپراسمولار هیپرگلیسمیک که قبلاً شوک یا کومای هایپراوسمولار نامیده میشد: مشخصه اصلی این عارضه هایپراوسمولاریتی خون است. این وضعیت شباهتهایی با کتواسیدوز دیابتی دارد با این تفاوت که وجود انسولین مانع از ایجاد کتونها و اسیدوز شدید میشود. در این وضعیت هایپرگلایسمی میتواند بسیار شدید و گاه بالای ۱۰۰۰ میلیگرم در دسیلیتر باشد. این وضعیت معمولاً در بیماران دیابت نوع دو دیده میشود، و معمولاً با وجود مقادیر بالای قند و نبود کتوز قابل توجه در حضور سایر علایم بالینی تشخیص داده میشود. در این بیماران دهیدراتاسیون شدیدتر است و متناسب با افزایش اوسمولاریته پلاسما سطح هوشیاری کاهش پیدا میکند. در این عارضه علایم عصبی شامل تشنج و وضعیتی شبیه سکته مغزی مشاهده میشود که با تصحیح اوسمولاریتی بهبود مییابد. درمان این وضعیت مرگبار باید تهاجمی باشد و شامل تجویز مایعات و انسولین است.
هیپوگلیسمی یا افت گلوکز خون: افت قند به مقادیر کمتر از مقادیر طبیعی (۳٫۳ میلیمول در لیتر) که در واقع عارضه ناشی از داروهای کاهش دهنده قند خون است. این عارضه میتواند در پی افزایش مصرف گلوکز در موقعیتهایی همچون ورزش زیاده از حد، کمبود دریافت غذایی یا مصرف مشروبات الکلی ایجاد شود، این وضعیت میتواند شدید باشد و به کما یا تشنج منجر شود. وجود احتمال بروز این عارضه پایین آوردن انتظارات درمانی برای کنترل گلوکز خون را الزامی میکند. همچنین بروز آن باعث ایجاد ترس در بیمار نسبت به تکرار عارضه و بیتوجهی به کنترل قند میشود؛ لذا در درمان دیابت توجه جدی میشود که از این عارضه پیشگیری شود. در صورت بروز درمان بسته به شدت علایم میتواند با مصرف خوراکی یا تزریقی قند و انجام اقدامات تشخیصی و تعیین قند خون صورت گیرد.
مزمن
عوارض دیابت بطور عمده به دو دسته تقسیم میشود:
عوارض میکروواسکولار
شامل رتینوپاتی (نابینایی)، نفروپاتی (آسیبهای گلومرول و دفع آلبومین) و نوروپاتی (کاهش یا ازدست دادن حس درد) است.
نفروپاتی دیابتی و بیماریهای کلیه: بیماریهای کلیه از یافتههای شایع در دیابتیها است. حدود نیمی از بیماران دیابتی در طول عمر خود علایم صدمه کلیوی را نشان میدهند. بیماری کلیه عارضه جدی است که میتواند منجر با کاهش طول و کیفیت عمر شود. نفروپاتی دیابتی شایعترین عارضه کلیوی دیابت است. نفروپاتی دیابتی به افزایش پیشرونده دفع پروتئین از ادرار (پروتئینوری) گفته میشود که در بیماران مزمن دیابتی دیده شده و منجر به کاهش عملکرد کلیه و در نهایت نارسایی کلیه میشود. عوامل خطر نفروپاتی دیابتی عبارت است از: طول مدت ابتلا به دیابت، کنترل قند ضعیف، فشار خون بالا، جنسیت مذکر، چاقی و مصرف سیگار. نفروپاتی مراحلی دارد که برای غربالگری، تشخیص و تعیین پروگنوز بیماری کاربرد دارد. در ابتدا بیماران دیابتی دفع طبیعی آلبومین دارند. در مراحل اولیه بروز نفروپاتی دفع پروتئین آلبومین در مقادیر اندک (میکروآلبومینوری) از ادرار ایجاد میشود. میزان دفع به تدریج افزایش مییابد تا در طی پیشرفت نفروپاتی به دفع واضح پروتئین از ادرار منجر شود. عبور از هر یک از این مراحل حدود پنج سال به طول میانجامد. در اواخر این روند سرعت افت عملکرد کلیه افزایش مییابد و لذا نارسایی کلیه در مراحل آخر بیماری آشکار میشود.
علاوه بر نفروپاتی دیابتی، این بیماران ممکن است سایر بیماریهای کلیه همچون نفروپاتی ناشی از فشار خون و نفروپاتی ایسکمیک را دچار شوند. این بیماریها بهطور مستقل یا همزمان با نفروپاتی دیابتی اتفاق میافتند. بعضی مطالعات مطرح کردهاند که در نیمی از بیماران دیابتی دچار نارسایی کلیوی آلبومینوری وجود ندارد. این مسئله اهمیت توجه به سایر ارزیابیهای عملکرد کلیه علاوه بر آلبومین ادرار را مطرح میکند.
رتینوپاتی دیابتی: دیابت میتواند باعث نابینایی شود، رتینوپاتی دیابتی شایعترین علت موارد جدید نابینایی در افراد مسن رتینوپاتی دیابتی است. کاهش بینایی همچنین با عوارض دیگری شامل افتادن، شکستگی استخوان ران و افزایش چهار برابر مرگ و میر همراه است. بهطور کلی رتینوپاتی دیابتی به سه شکل دیده میشود: ۱-آدم ماکولا (نشت عروقی منتشر یا موضعی در ماکولا) ۲-تجمع پیشرونده عروقی (میکروآنوریسم، خونریزیهای داخل شبکیه، خمیدگی عروقی، مالفورماسیونهای عروقی (رتینوپاتی دیابتی غیر پرولیفراتیو) و ۳-انسداد شریانی شبکیه در مراحل آخر.
نوروپاتی دیابتی: بیماران دیابتی ممکن است دچار طیف گستردهای از اختلالات چندگانه اعصاب شوند که انواع اعصاب مختلف حسی و حرکتی را میتواند درگیر کند. این عارضه معمولاً طی ۱۰ سال از بروز بیماری در ۴۰ تا ۵۰ درصد از دیابتیها مشاهده میشود. افراد مبتلا شده به دیابت نوع یک تا پنج سال پس از بروز بیماری ممکن است دچار نوروپاتی نشوند اما در دیابت نوع دو ممکن است این عوارض از همان ابتدا وجود داشته باشند. فاکتورهای خطری که ریسک بروز نوروپاتی را در دیابتیها افزایش میدهند عبارتند از: افزایش میزان قند خون، افزایش تریگلیسیرید خون، شاخص توده بدنی بالا، مصرف سیگار و فشار خون بالا. زخم پای دیابتی تا حدود زیادی وابسته به نقص حسی ناشی از نوروپاتی دیابتی است که خود عارضه جدی است و میتواند منجر به قطع عضو شود. از مشکلات دیگر در نوروپاتی دیابتی دردهای نوروپاتیک است که ناشی از اختلال در اعصاب سمپاتیک است و میتواند مشکلات بسیاری برای بیمار و درمانگر ایجاد کند که شامل انواع پلی نوروپاتی یا مونونوروپاتی میباشد. از پلی نوروپاتیها میتوان به پلی نوروپاتی دیستال متقارن، پلی رادیکولوپاتی اشاره کرد. تشخیص زودرس نوروپاتی اهمیت زیادی در پیشگیری از عارضههای آن دارد.
عوارض ماکروسکولار
بیماران دیابتی از افزایش قابل توجه ریسک ابتلا به بیماریهای قلبی عروقی آترواسکلروزی رنج میبرند. این شامل سکته مغزی، بیماری عروق کرونر و بیماریهای عروق محیطی است. ریسک این بیماریها در هر دو نوع اصلی دیابت و حتی در سنین پایین افزایش یافتهاست. مشخص شدهاست که در افراد دیابتی جوان ریسک بروز سکته زودرس بیشتر از افراد سالم است.
بیماری عروق کرونر: علت اصلی مرگ و میر در بیماران دیابتی بیماریهای قلبی است. ۶۵ تا ۸۰ درصد از دیابتیها در اثر بیماریهای قلبی میمیرند. بیماران دیابتی در ریسک بالاتری از بیماریهای قلبی هستند و این مشکلات در سنین پایینتری ایجاد میشود. بیماران دیابتی همچنین ریسک بالاتر ابتلا به ایسکمی قلبی ساکت دارند و یک سوم از سکتههای قلبی در این بیماران بدون علایم شناخته شده سکته اتفاق میافتد.
سکته مغزی: دیابت یکی از ریسک فاکتورهای قابل تغییر مهم در اولین سکته ایسکمی مغزی است. دیابت ریسک سکته مغزی را در مردان ۲–۳ برابر و در زنان ۲–۵ برابر افزایش میدهد. دیابت همچنین ریسک بروز مجدد سکته مغزی را دو برابر افزایش میدهد. عوارض سکته مغزی در دیابتیها بدتر از سایر افراد است که این شامل هزینههای بیمارستانی، معلولیتها و نواقص عصبی باقیمانده، و مرگ و میر در بلندمدت میشود.
بیماری عروق محیطی:دیابت اولین علت قطع عضو غیرتروماتیک اندام تحتانی به حساب میآید. زخم پا در حدود۱۵٪مبتلایان به دیابت نوع دو ایجاد میگردد و شایعترین محل آن شست پا میباشد. در جنس مذکر، دیابت طول کشیده بیشتر از ده سال، نوروپاتی محیطی، سیگارکشیدن، بیماری عروق محیطی و سابقه قطع عضو قبلی یا زخم بیشتر مشاهده میگردد.
ریسک فاکتورها و غربالگری
دیابت نوع یک
ریسک بروز دیابت یک را میتوان با بررسی سابقه خانوادگی این بیماری و توجه به سن بروز و جنسیت اعضا درگیر خانواده تخمین زد. همچنین راههای دیگری هم برای پیشبینی بروز دیابت نوع یک ارائه شدهاست ولی از آنجا که هنوز راهی برای پیشگیری یا متوقف کردن روند بیماری وجود ندارد استراتژیهای مختلفی که برای تشخیص زودرس دیابت نوع یک وجود دارد ارزش زیادی ندارند.
دیابت نوع دو
دیابت نوع دو تشخیص داده نشده یکی از مشکلات رایج در سیستمهای درمانی است. استفاده از آزمایشهای ساده قند میتواند این افراد را که در معرض دچار شدن به عوارض قابل پیشگیری دیابت هستند تشخیص دهد. آزمون غربالگری مورد استفاده برای تشخیص دیابت آزمون قند ناشتای خون و هموگلوبین A1C است. در صورتی که میزان قند ناشتا یا A1C در حد نزدیک به دیابت باشد انجام آزمایش تحمل قند ۷۵ گرمی نیز توصیه میشود. افرادی که در پی این آزمایشها قند بالایی داشته باشند ولی هنوز به میزان تشخیصی دیابت نرسیده باشند به عنوان اختلال تحمل گلوکز طبقهبندی میشوند. مشخص شده که این افراد هم در معرض عوارض ماکروسکولار دیابت به خصوص در زمینه سندرم متابولیک قرار دارند.
ریسک فاکتورهای دیابت نوع دو
سن بالای ۴۰ سال
فامیل درجه اول مبتلا به دیابت نوع ۲
سابقه اختلالات قند پیشدیابتی (اختلال تحمل گلوکز، گلوکز ناشتای مختل
سابقه دیابت بارداری
سابقه به دنیا آوردن نوزاد ماکروزوم (وزن بالاتر از حد طبیعی)
وجود عوارض انتهایی دیابت روی اعضا بدن
وجود فاکتورهای خطر بیماریهای قلبی عروقی (همچون چربی خون بالا، فشار خون بالا، چاقی)
وجود بیماریهای مربوط به دیابت (سندرم تخمدان پلیکیستیک، آکانتوز نیگریکانز، عفونت اچ.آی. وی، برخی اختلالات روانپزشکی همچون شیزوفرنی، افسردگی و اختلال دوقطبی)
مصرف داروهای مربوط به دیابت: کورتیکواستروئیدها، آنتیسایکوتیکهای آتیپیک، درمان اچآیوی/ایدز و غیره.
تشخیص
بر اساس آخرین معیارهای انجمن دیابت آمریکا تشخیص دیابت با ثبت یکی از موارد زیر قطعی است:
ثبت حداقل یک میزان قند خون تصادفی بالای ۲۰۰ میلیگرم بر دسیلیتر به همراه علایم کلاسیک دیابت (پرنوشی، پرادراری، پرخوری)
قند ناشتای پلاسمای بالاتر یا مساوی ۱۲۶ میلیگرم بر دسیلیتر (ناشتا به معنای هشت ساعت عدم مصرف هر نوع کالری قبل انجام آزمایش است)
هموگلوبین A1C بالای ۶٫۵٪
نتیجه آزمایش تحمل قند ۷۵ گرمی خوراکی دو ساعته بالای ۲۰۰ میلیگرم بر دسیلیتر
اختلالات پیشدیابتی
در بیماران دیابت نوع دو، بیماری دیابت به تدریج و در عرض چندین سال بروز میکند. بیماران قبل از رسیدن به دیابت آشکار و واضح از یک مرحله مقدماتی بدون علامت عبور میکنند. این گروه «پیش دیابتی» (prediabetes) را برخی از منابع تحت عنوان افراد با «خطر افزایش یافته دیابت»(increased risk of diabetes) نامگذاری مینمایند و WHO یا سازمان بهداشت جهانی آنان را افراد با «هیپرگلیسمی بینابینی»(intermediate hyperglycemia) مینامد.
در این گروه از بیماران، معیارهای مربوط به تشخیص بیماری دیابت، یعنی قند خون ناشتا (fasting plasma glucose FPG) یا هموگلوبین A1C یا مقادیر تست تحمل خوراکی قند (oral glucose tolerance test OGTT) از یک طرف از مقادیر نرمال مربوطه بالاتر است و از طرف دیگر به حد لازم برای تشخیص بیماری دیابت شیرین نیز نمیرسد. بر این اساس در هر یک از روشهای سه گانهٔ تشخیص دیابت، ما با گروهی برخورد میکنیم که در بینابین مقادیر نرمال تا مقادیر دیابتی قرار دارند.
در خصوص قند خون ناشتا، مقدار نرمال زیر ۱۰۰ میلیگرم در دسیلیتر است و حد لازم برای تشخیص دیابت ۱۲۶ میلیگرم در دسیلیتر است و از این رو بیمارانی که قند خون ناشتای آنان در مقادیر ۱۰۰ تا ۱۲۵ میلیگرم در دسیلیتر قرار دارد این گروه از بیماران اختلال پیش دیابتی، با عنوان «اختلال قند ناشتا» (Impaired fasting glucose IFG) نامیده میشوند.
در هموگلوبین A1c مقادیر نرمال زیر ۵٫۶٪ است و حد نصاب تشخیص دیابت بزرگتر مساوی ۶٫۵٪ است و لذا افرادی که مقادیر بین ۵٫۷٪ تا ۶٫۴٪ را دارند، جزو گروه پیش دیابتی قرار میگیرند.
در تست تحمل قند، مقادیر نرمال قند خون، دو ساعت بعد از خوردن ۷۵ میلیگرم قند، کمتر از ۱۴۰ میلیگرم در دسیلیتر است در حالیکه برای تشخیص دیابت این مقدار باید بزرگتر یا مساوی ۲۰۰ میلیگرم در دسیلیتر باشد و به همین سبب این زیرگروه از بیماران پیشدیابتی که مقادیر این آزمایش آنان بین ۱۴۰ تا ۱۹۹ میلیگرم در دسیلیتر باشد را به نام «اختلال تحمل قند»(impaired glucose tolerance IGT) مینامند.
نکته مهم انست که افراد این سه گروه فوق لزوماً برهم منطبق نمیباشند، به عبارتی ممکن است فردی قند خون ناشتای وی در حد نرمال باشد ولی با تست تحمل قند، در گروه پیش دیابتی قرار گیرد.
نکته بعدی انست که در میدان عمل بالینی، استفاده از تست تحمل قند، هرچند ابزار دقیقی است، نه برای تشخیص دیابت و نه برای تشخیص پیش دیابتی بطور معمول توصیه نمیشود و از ان بیشتر برای انجام امور تحقیقاتی و اپیدمیولوژیک استفاده میگردد و معیارهای فعلی به استفاده از قند خون ناشتا یا هموگلوبین A1c به عنوان مناسبترین تست در افراد بدون علامت تأکید دارند.
اما مهمترین موضوع در بیماران پیش دیابتی فرجام آنان و نحوه برخورد با این اختلال است. بیماران دیابت نوع دو قبل از ابتلا به بیماری دیابت باید از مرحله پیش دیابتی عبور نمایند و لذا این یک شانس را به این گروه در معرض خطر میدهد که با برخورد مناسب بتوانند جلوی پیشرفت دیابت را بگیرند. امروزه در خصوص درمان دارویی این بیماران اختلاف نظر وجود دارد. انجمن دیابت آمریکا ADA میگوید اگر فرد پیشدیابتی دارای معیارهای خطر بالا باشد، (شاخص توده بدنیBMI بالای ۳۵، سابقه خانوادگی دیابت در بستگان درجه اول یا خانمی که خود سابقهای از دیابت بارداری دارد)، بهتر است با متفورمین برای جلوگیری از بروز بیماری دیابت درمان شوند. اما اکثر افراد این معیارها را ندارند و برای آنان این نکته مورد توافق همگان میباشد که باید سبک زندگی خود را تغییر دهند. لازم است این افراد برنامهٔ مدونی برای کاهش وزن داشته باشند و همچنین افزایش فعالیت فیزیکی به صورت ورزش منظم حداقل ۵ بار در هفته را پیشه نمایند. این بیماران همچنین باید بطور سالیانه از نظر ابتلا به بیماری دیابت مورد آزمایش قرار گیرند و در عین حال این افراد علاوه بر دیابت، در خطر بالاتری برای بیماریهای قلبی عروقی نیز قرار دارند و لذا لازمست که از نظر بیماریهای قلبی عروقی مورد غربالگری منظم قرار گیرند.
پیشگیری
برای پیشگیری از تشکیل زخمهای دیابتی راههای مختلفی وجود دارد که عبارتند از: پرهیز از سیگار، تحت کنترل داشتن قند و فشار خون و کلسترول، ورزش برای تحریک جریان خون، تمیز نگه داشتن پاها، بررسی کردن هر روز پاها به منظور یافتن خراش و ترک خوردگی پوست، خشک کردن پاها بعد از حمام.
کنترل میزان قند خون از مهمترین موضوعها در برخورد با بیماری دیابت است. به تازگی محققان دانشگاه لیدز آمریکا با استفاده از فناوری لیزر موفق به تولید یک دستگاه غیرتهاجمی شدهاند که قندخون دیابتی را کنترل میکند. این سیستم GlucoSense نام دارد و بدون هیچ سوزن یا جراحی، قندخون را بهطور مداوم اندازهگیری میکند. در این روش، بیمار انگشت خود را روی حسگر شیشهای کوچکی قرار میدهد. در این هنگام، یک پرتو لیزر کم توان به انگشت تابیده میشود. بخشی از این پرتو توسط گلوکز خون جذب و باقیمانده به حسگر شیشهای بازتاب میشود.
ورزش و دیابت
ورزش به دیابتیها کمک میکند که از شر حملههای قلبی و نابینایی و آسیبهای عصبی در امان باشند. وقتی که غذا میخورید سطح قند خونتان افزایش مییابد. هر چه بیشتر سطح خون افزایش یابد قند بیشتری به یاختهها میچسبد. وقتی که قند به یاخته بچسبد دیگر نمیتواند از آن جدا شود و تبدیل به مادهای زیانآور به نام سوربیتول میشود که این ماده میتواند باعث نابینایی و ناشنوایی و آسیبهای مغزی و قلبی و نشانگان پاهای سوزان و… گردد.
وقتی که قند وارد بدن شما میشود فقط میتواند در یاختههای کبد و ماهیچه ذخیره گردد. اگر یاختههای کبد و ماهیچه از کربوهیدرات اشباع باشند، قندها دیگر جایی برای رفتن ندارند. اگر ذخیره یاختههای ماهیچه در پی ورزش کردن مصرف گردد پس از صرف غذا قندها به وسیله ماهیچه جذب میشوند و مقدار آنها در خون افزایش نمییابد؛ بنابراین اگر با یک برنامه ورزشی منظم بتوانیم ذخیره قند ماهیچهها را کاهش دهیم مسلماً میتوانیم شاهد بهبود همهجانبه عوارض بیماری دیابت باشیم.
زخمهای دیابتی
زخمهای دیابتی، جراحتهایی در پوست، چشم، اعضای موکوسی یا یک تغییر ماکروسکوپی در اپیتلیوم نرمال افراد دیابتی تیپ ۱ و ۲ میباشد. بیش از ۷۵ ٪ افراد دیابتی، مبتلا به زخمهای دیابتی هستند که در آمریکا بیش از ۸۰ ٪ آنها منجر به قطع عضو میشوند که در صورت مراجعه به خوبی درمان میشدند. زخمها در هنگام بروز، مستعد عفونت هستند (اگرچه عفونت به ندرت در اتیولوژی زخمهای دیابتی دخالت دارد). این جراحتها معمولاً به دلیل زخمهای اولیه، التهاب، عفونت یا شرایط دارویی ایجاد میشوند که سلامتی را بهخطر میاندازند. بهطور کلی افرادی با سابقه دیابت بیش از ۱۰ سال، جنس مذکر (مردها)، عوارض قلبیعروقی، عوارض کلیوی، بیشتر از دیگر بیماران دیابتی، در معرض خطر زخم پای دیابتی میباشند. دیگر دلایل ایجاد این زخمها شامل عفونت ثانویه (باکتری، قارچ یا ویروس) و ضعف شدید بیمار میباشند.
علایم زخم دیابتی
علایم شایع در عفونتهای پای دیابتی شامل موارد زیر است:
میخچه، کالوس
ناهنجاریهای استخوان پا* تب، قرمزی، آدم یا دیگر علایم عفونت
بافتی که روی محل جدید عفونت به وجود(scar) میآید
زخمهای پا که در ا ثر آسیب عصبی یا جریان خون ضعیف به وجود میآیند (زخمها اغلب بالای قوزک یا زیر شست یا در محلی از پا که ناشی از نامناسب بودن کفش است، تشکیل میشود).
تغییر شکل عضلات، پوست یا استخوان پا در اثر آسیب عصبی و گردش خون ضعیف
کند بودن مراحل بهبود زخم
پینه بستن پا و انگشتان چماقی
درمان
درواقع درمانی قطعی برای دیابت وجود ندارد و تنها میتوان آن را کنترل کرد که در مراحل حاد قرار نگیرد. جایگزینی سلولهای β از دست رفته، نقش بسزایی در تنظیم قند خون و کاهش اختلالات دیابتی دارد. در طی دهههای گزشته استراتژیهای مختلفی برای جایگزینی سلولهای β از دست رفته به کار گرفته شد. پیوند جزایر لانگرهانس پانکراس یکی از این راهکارها میباشد که بهطور موفقیتآمیزی در کلینیک صورت گرفتهاست. اما در عمل به دلیل کمبود افراد دهنده پیوند و چالش بر سر سرکوب سیستم ایمنی فرد دریافتکننده محدود گشت.
از راهکارهای دیگر، جایگزینی سلولهای β از دست رفته از طریق سلولهای α پانکراسی میباشد (تمایز سلولهای α به β پانکراس). فاکتور رونویسی Arx، یکی از فاکتورهای مهمی است که در حین تشکیل پانکراس باعث تفاوت سرنوشت سلولهای α و β پانکراسی میشود. بیان این فاکتور رونویسی باعث تبدیل سلولهای پیش ساز اندوکراینی پانکراس به سلولهای α میگردد. این فاکتور با سرکوب بیان فاکتور رونویسی Pax4 باعث بیان فاکتورهای زیردست اختصاصی سلولهای α میگردد. عدم بیان Arx و بیان Pax4 باعث ایجاد سلولهای β پانکراسی میشود؛ بنابراین مطالعه بر روی حذف ژن Arx و در نتیجه بیان Pax4 زمینه مطالعاتی محققان را برای جایگزینی سلولهای β فراهم کرد.
با این حال به نظر میرسد که فاکتورهای رونویسی تنها فاکتورهای دخیل در تمایز سلولهای α به β نیستند. در مطالعهای که در این راستا انجام شد از سلولهای بنیادی برای ایجاد سلولهای β تولیدکننده انسولین استفاده شد. اما مشاهدات حاکی از این بود که این سلولها توانایی پاسخ گویی به محرک خارج سلولی گلوکز را ندارند. با وارد کردن این سلولها به بدن موش و بلوغ این سلولها به مدت پنج ماه، این سلولها توانایی بالانس قند خون را نسبت به محرک خارج سلولی گلوکز پیدا میکنند. به نظر میرسد که تغییرات اپی ژنتیکی نقش قابل ملاحظهای در تعیین سرنوشت سلولهای اندوکراینی و بلوغ کامل آنها دارد. بعبارتی فاکتورهای رونویسی و تغییرات اپی ژنتیکی هردو با همکاری هم نقش در تعیین سرنوشت یک سلول و بروز ویژگی اختصاصی برای آن سلول دارند.
متیلاسیون DNA از جمله تغییرات اپی ژنتیکی است که در بقای یک سلول نقش دارد. مطالعات اخیر نشان داده که نقش متیلاسیون در سلولهای α پانکراسی تنها در بقای سلولی خلاصه نمیشود. در این سلولها متیلاسیون DNA باعث حفظ ویژگی اختصاصی سلولهای α و تمایز آنها از سایر سلولهای اندوکراینی میگردد.
Dnmt1 یکی از آنزیمهایی است که در متیلاسیون DNA نقش دارد و محققان به مطالعه همزمان این آنزیم و فاکتور رونویسی Arx برای تمایز سلولهای α به β میپردازند.
حذف فاکتور رونویسی Arx به تنهایی باعث تبدیل ۳۰٪ از سلولهای α به سلولهای مشابه β بعد از ۱۲ هفته میشود. اما سلولهای جدید تولید شده مارکرهای اختصاصی بلوغ سلولهای β را ندارند. در مقابل با حذف Dnmt1، هیچیک از فاکتورهای اولیه اختصاصی سلولهای β بعد از ۱۰ ماه مشاهده نشد. در مرحله بعد، حذف هردو فاکتور Arx و Dnmt1 صورت گرفت. در هفته ۱۲ ام از حذف این دو فاکتور بیش از ۵۰٪ از سلولهای α، توانایی تولید انسولین را پیدا کردند و بیان فاکتورهای اختصاصی مرتبط با بلوغ سلولهای β مشاهده شد. نکته قابل توجه این است که سلولهای β جدید تولید شده از لحاظ خواص فیزیولوژی نیز مشابه سلولهای β اصلی میباشند. در نتیجه این تحقیقات اهمیت دو فاکتور Arx و Dnmt1 در حفظ ویژگی سلولهای α مشخص گردید و نشان داده شد که حذف این دو فاکتور در بروز ویژگیهای اختصاصی سلولهای β دخیل است.
برای زخم دیابت نیزمیتوان درمان را درنظر گرفت. درمان زخمهای دیابتی به طرق مختلف انجام میگیرد:
مراقبت پا: که شامل مرطوب نگه داشتن محیط زخم با ا انتخاب ماده مناسب، همچنین خشک نگه داشتن لبههای زخم. در بیماران دیابتی وابسته به انسولین که مبتلا به زخم هستند، مراقبتها حدود ۳ سال ادامه مییابد.
آنتیبیوتیکها: آنتیبیوتیکها حتی زمانی که عفونتها بروز نکردهاند (پروفیلاکتیک) تجویز میشوند تا از بروز عفونت جلوگیری شود.
کنترل قند خون: یکی از عوامل ایجاد زخمهای دیابتی، بالا بودن قند خون است. بالا بودن قند خون ایمنی را کاهش میدهد و بهبودی زخم را به تأخیر
میاندازد. کنترل قند خون چه به صورت تجویز دارویی و چه به صورت غذایی و همچنین تجویز انسولین به صورت کوتاه مدت زخم را بهبود میبخشد و قند اولیه را کنترل میکند.
پیوند پوست: پیوند پوست نیز میتواند زخمهای دیابتی را درمان کند.
جراحی: برداشت بافت مرده اطراف محل زخم معمولاً برای تمیز کردن و بهبودی زخمها انجام میشود. جراحی بای پس، جریان خون را در شریان پا بهبود میبخشد که ممکن است در التیام زخم و جلوگیری از قطع عضو کمککننده باشد و در پایان قطع عضو برای متوقف کردن گسترش عفونت نیاز است.
اکسیژن درمانی هایپر باریک: افزایش ۵ برابر غلظت O از ۲۰ ٪ تا ۱۰۰ ٪ و افزایش فشار آن از ۱ اتمسفر به ۲ اتمسفر در مجموع منجر به ۱۰ برابر شدن میزان اکسیژن میشود که یکی از اثرات آن به وجود آمدن رگهای خونی بیشتر در محل میباشد که منجر به کاهش جریان خون و مناسب تر شدن جریان به مناطقی که بلوک خونی دارند میگردد. به نظر میرسد درمان اکسیژن هایپر باریک به کاهش قطع عضو کمک میکند.
محققان آمریکایی اعتقاد دارند درمان رایج دیابت میتواند با روند درمان پیری، به بزرگسالان کمک کند تا ۱۲۰ سالگی خوب زندگی کنند.
بسیاری از افراد پس از آغاز درمان و استفاده از دارو حتی از قبل هم چاقتر میشوند و این بدان علت است که فرد دیابتی کنترلی بر روی عادتهای غذایی خود ندارد و حتی داروهایی که برای درمان فرد استفاده میشود نمیتوانند کارای مورد نظر را داشته باشند تا زمانی که عادتهای غذایی درست دنبال شود و به همین علت فرد دچار اضافه وزن و چاقی میشود. لوزالمعده به منظور جلوگیری از افزایش ناگهانی قند خون پس از صرف غذا مقداری انسولین در خون وارد میکند و انسولین با راندن قندها به درون یاختهها از وقوع این امر جلوگیری میکند. اما انسولین و تمام داروهایی که از آن ساخته میشوند باعث میشوند که شما همواره احساس گرسنگی کنید، بنابراین در تجویز انسولین سعی این است که با کمترین میزان مصرف انسولین بتوانیم از بالا رفتن قند خون جلوگیری به عمل بیاوریم.
پرهیز غذایی
بسیاری از افرادی که بعد از سن ۴۰ سالگی دچار دیابت میگردند با رعایت یک رژیم غذایی مشتمل بر مصرف سبزیجات، غلات کامل، حبوبات و ماهی و محدود کردن شدید فراوردههای شیرینیپزی و شکر و محدود کردن دریافت کربوهیدرات میتوانند حال خود را بهبود بخشند. بسیاری از کسانی که دچار دیابت شدهاند انسولین مصرف میکنند آنها توانایی کافی برای پاسخ دادن به انسولین را ندارند و این امر به علت وزن بالا و مصرف زیاد قندهای تصفیه شده از سوی آنهاست. اولین دستور برای برطرف کردن این حالت استفاده از غلات و دانههای کامل به جای فراوردههای شیرینی و نانپزی (آرد سفید) است. این امر با کمک به احساس سیری و خوردن کمتر باعث محدود کردن دریافت مهمترین منبع دریافت چربیها خواهد گردید. طبق نظر پزشکی گیاهی برای کنترل دیابت میتوان از عرقیات گیاهی همچون:۱- شنبلیله ۲- برگ زیتون ۳- ماستیک ۴- مارتیغال ۵- دارچین ۶- فلفل قرمز ۷- برگ گردو ۸- گزنه و… استفاده کرد؛ و موادی مانند نان سبوس دار و سیب و انار و گردو در درمان دیابت نقش دارند.
برپایه پژوهشهایی که در اروپا انجام گرفتهاست نشان داده شده که دریافت مقادیر بسیار زیاد پروتئین به کلیههای یک فرد دیابتی آسیب وارد میکند بنابراین دیابتیها باید از مقادیر کمتر گوشت و ماکیان و تخم مرغ استفاده نمایند. همچنین تحقیقات اخیر نشان میدهد که کربوهیدراتهای تصفیه شده میزان نیاز به انسولین را افزایش و چربیهای غیر اشباع تکپیوندی و چندپیوندی موجود در سبزیجات و چربیهای امگا-۳ موجود در روغن ماهی و همچنین استفاده از آرد کامل و دانههای کامل به جای آرد تصفیه شده نیاز به انسولین را کاهش میدهد. سطح بالای قند خون بعد از صرف غذا موجب میشود که قندها به یاختهها چسبیده و تبدیل به مادهای سمی (برای یاختهها) به نام سوربیتول شوند که این ماده به اعصاب و کلیه و رگها و قلب آسیب خواهد رساند.
نقش ویتامینها در دیابت
نقش ویتامینها در دیابت از دیرباز مورد بحث بودهاست و تاکنون برای آنها نقش معینی مشخص نشدهاست. همواره سؤال این بوده که اگر در مواردی همراهی دیابت با اختلالات ویتامینی دیده میشود، ایا این رابطه به صورت رابطه علت و معلولی است یا خیر و اگر فوایدی در مصرف ویتامین دیده میشود، ایا به دلیل آثار آنتیاکسیدان انهاست یا به دلیل اثر مستقیم آنها در دیابت و اینکه ایا این اثر تنها در افراد خاصی ظاهر میگردد یا اینکه در تمام بیماران دیابتی مفید است. بسیاری از بیماران ویتامینها را استفاده مینمایند و گروهی از پزشکان آن را پیشنهاد میدهند و بعضی از بیماران فوایدی نیز برای ان ذکر میکنند ولی این توصیهها هنوز اعتبار قطعی علمی ندارد.
مطالعات نشان داده که کمبود ویتامین دی (D) همراه ازدیاد خطر بروز دیابت است ولی در عین حال مصرف ویتامین دی (D) به صورت کمکی اثری در کاهش بروز دیابت نداشتهاست. متا آنالیز یکسری از مطالعات نشان داد که قدرت ویتامین د (D) در پیشگیری از دیابت نوع یک وابسته به دوز و مدت مصرف انست لذا مطالعاتی در این خصوص انجام شد. یک مطالعه نشان داد که مصرف روزانه ۲۰۰۰ واحد ویتامین دی (D) در طی اولین سال زندگی در شیرخواران با کاهش خطر بروز دیابت نوع یک همراه است ولی نتوانستند یک رابطه علت و معلولی را اثبات نمایند. در مطالعه دیگری مصرف ۲۰۰۰ واحد در روز ویتامین د۳ (D3) با مصرف روزانه ۴۰۰ واحد که دوز معمول ان است مورد مقایسه قرار گرفت ولی در این بررسی کودکانی وارد مطالعه شده بودند که دارای استعداد ژنتیکی بالایی برای دیابت بودند و لذا قابل تعمیم به کودکان عادی نمیباشد. با این وجود بعضی منابع مصرف ویتامین دی (D) را توصیه ضمنی میکنند مثلاً یکی از منابع اندوکرینولوژی (غدد درونریز) مینویسد: «در بعضی مطالعات ثابت شده که ویتامین دی (D) مقاومت به انسولین را کم کرده و در کاهش وزن و کنترل اشتها نیز مفید است» هر چند که منابع این استدلال خود را ذکر نکردهاست.
ویتامین ب۳ (B3) یا نیکوتین امید در یک مطالعه اروپایی به نام «آزمایش اروپایی مداخله در دیابت بتوسط نیکوتینامید»(European Nicotinamide Diabetes Intervention Trial ENDIT) مورد آزمایش قرار گرفت و هیچگونه اثر مفیدی از خود در دیابت نشان نداد.
رابطه دیابت و ویتامین آ (A) مدت مدیدی مورد مجادله بودهاست. اولین بار در سالهای ۱۹۲۹ و ۱۹۳۰ دانشمندان متوجه این رابطه شدند و تاکنون بحث در این خصوص ادامه داشتهاست. اخیراً یک مطالعه نشان داد که سلولهای بتای پانکراس که محل تولید انسولین هستند، دارای گیرندههایی برای یک متابولیت ویتامین آ (A) به نام all-trans retinoic acid ATRA هستند و لذا برای ویتامین آ (A) یک رابطه علی با دیابت فرض شدهاست هر چند این نظریه نیاز به ارزیابی و تأیید دارد.
در عین حال گاهی در مطالعات سوگیری یا تورش هم دیده شدهاست. مثلاً یکسری از مطالعات فوایدی از آثار ویتامین ایی (E) یا ویتامین سی (C) در دیابت نشان دادهاند و دلیل آن را کاهش هموگلوبین A1C ذکر نمودهاند. هموگلوبین A1C ناشی از قنددار شدن یا گلیکاسیون (glycation) هموگلوبین است و هر چه قند خون بالاتر باشد، میزان هموگلوبین A1C نیز بالاتر میرود و بر عکس هر چه قند خون بهتر کنترل گردد، میزان هموگلوبین A1C پایینتر است به همین علت یکی از مهمترین آزمایشها در اثبات کنترل مناسب دیابت، میزان هموگلوبین A1C است. ویتامین ایی (E) یا ویتامین سی (C) هر دو از طریق واکنش شیمیایی و نه کم کردن قند خون، مانع گلیکاسیون (glycation) هموگلوبین میگردند لذا هر چند بظاهر مصرف آنان موجب کاهش هموگلوبین A1C شده و اینطور نتیجه گرفته شده که این ویتامینها موجب کاهش قند خون شدهاند ولی در حقیقت این امر ناشی از دخالت آنان در یک واکنش شیمیایی است و نه اثر بر قند خون و لذا این ویتامینها اثری واقعی در کاهش قند خون نداشتهاند. گاهی نیز موضوع برعکس است یعنی دیابت روی کاهش ویتامین اثر داشتهاست. مثلاً مصرف دراز مدت متفورمین که یکی از داروهای دیابت است، گاهی موجب کاهش ویتامین ب۱۲ (B12) میگردد.
نکتهای که باید در مطالعات به ان توجه نمود انست که فواید احتمالی مصرف ویتامینها، در افراد دارای کمبود ویتامین مورد نظر دیده شدهاست و این امر دلالتی بر توصیه به مصرف این ویتامینها در تمامی افراد دیابتی بدون کمبود آنها ندارد و به همین سبب است که معتبرترین مرجع دنیا مینویسد: «هیچ شواهد روشنی برای مفید بودن ویتامینها در دیابت در افرادی که کمبود ویتامینی ندارند، وجود ندارد» و سپس میگوید: «کاربرد روتین ویتامینهایی مثل ایی (E)، سی (C)، دی (D) و آ (A) در دیابت توصیه نمیشود چون هنوز شواهد کافی برای کارایی آنان در دسترس نمیباشد و خطرات احتمالی مصرف دراز مدت این فراوردهها نیز نامعلوم است.»
منبع دانشنامه آزاد